癌症干细胞靶向技术
1 癌症干细胞靶向技术
癌症治疗历史
癌症化疗,最早始于上世纪40年代用氮芥治疗淋巴瘤和用叶酸治疗儿童白血病,直到目前化疗仍是临床上癌症治疗的重要手段。癌症靶向治疗,从1997年由FDA批准的以CD20为靶点的Rituximab、1998年批准的以Her-2为靶点的Herceptin以及2001年批准的酪氨酸激酶抑制剂Imatinib开始,但现有靶向治疗药物对绝大多数癌症的疗效都很有限。癌症免疫治疗,则是从最近2015年以免疫检查点PD-1为靶点的Nivolumab和Pembrolizumab获得FDA批准的上市开始。目前癌症免疫治疗是癌症治疗的热点领域之一,但大多数癌症患者对免疫检查点抑制剂不敏感。因此,癌症治疗亟需研发创新药物。
癌症干细胞介绍
● 癌症复发和转移的根源
癌症的复发和转移是目前癌症临床治疗中面临的一项重大挑战1。现代科学认为,癌症干细胞(Cancer Stem Cell,CSC)是肿瘤细胞内部一小群极恶性的肿瘤细胞,是癌症复发和转移的“种子”2。尽管传统的化疗和放疗对大部分肿瘤细胞有效,但癌症干细胞则能耐受这些治疗,也是导致癌症复发和转移的重要根源之一3,4。此外,传统的化疗和放疗反而会增加普通肿瘤细胞的干细胞性潜能(Stemness potential),从而造成癌症干细胞的富集2,5。
强新科技是目前癌症干细胞靶向药物研发领域的全球领军企业。
● 癌症干细胞的特点
癌症干细胞具有以下三个关键特征:
1)干细胞性潜能--自我更新及再生肿瘤细胞的能力
2)对化疗的抗药性与放疗的不敏感性
3)导致癌症复发和转移
参考文献
-
Li Y, Rogoff HA, Keates S, Gao Y, Murikipudi S, Mikule K, Leggett D, Li W, Pardee AB, Li CJ. Suppression of cancer relapse and metastasis by inhibiting cancer stemness. Proc Nat Acad Sci USA. 2015;112(6):1839-1844.
-
Hu X, Ghisolfi L, Keates AC, Zhang J, Xiang S, Lee DK, Li CJ. Induction of cancer stemness by chemotherapy. Cell Cycle. 2012;11(14):2691-2698.
-
Jordan CT, Guzman ML, Noble M. Cancer stem cells. N Engl J Med. 2006;355(12):1253-1261.
-
Boman BM, Huang E. Human colon cancer stem cells: a new paradigm in gastrointestinal oncology. J Clin Oncol. 2008;26(17):2828-2838.
-
Ghisolfi L, Keates AC, Hu X, Lee DK, Li CJ. Ionizing radiation induces stemness in cancer cells. PLoS ONE. 2012;7(8):ea43628.
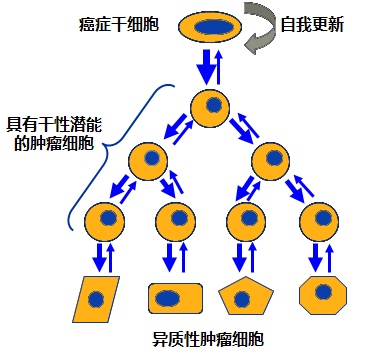
1.1干细胞性潜能:自我更新及分化能力
癌症干细胞具有干细胞性潜能,能自我更新及分化形成异质性的大量肿瘤细胞1。尽管癌症干细胞在全部肿瘤细胞中只占少数2,但可产生大量能构成肿瘤的主体部分的异质性肿瘤细胞1。
癌症干细胞还具有向远处转移的能力,并能保持它们的干细胞性特征,从而导致肿瘤在转移部位再生3。
癌症干细胞的干细胞性与调控肿瘤生长及向远处转移的相关信号通路失调密切相关。
参考文献
-
Gupta PB, Chaffer CL, Weinberg RA. Cancer stem cells: mirage or reality? Nat Med.2009;15(9):1010-1012.
-
Clarke MF. Self-renewal and solid-tumor stem cells. Biol Blood Marrow Transplant.2005:11(2 suppl 2):14-16.
-
Jordan CT, Guzman ML, Noble M. Cancer stem cells. N Engl J Med. 2006;355(12):1253-1261.
-
Li Y, Rogoff HA, Keates S, Gao Y, Murikipudi S, Mikule K, Leggett D, Li W, Pardee AB, Li CJ. Suppression of cancer relapse and metastasis by inhibiting cancer stemness. Proc Nat Acad Sci USA. 2015;112(6):1839-1844.
1.2 对传统治疗的不敏感性或抗药性
目前从各种类型的癌症中均已分离鉴定出癌症干细胞。研究表明癌症干细胞对传统化疗和放疗具有很强的耐受能力1。因此,目前靶向肿瘤细胞的治疗策略虽短期能有效缩减肿瘤体积,但对癌症干细胞却无效2。相反,有证据表明化疗或放疗反而会富集癌症干细胞3,4。肿瘤微环境和干性信号通路的失调是癌症干细胞能耐受放疗和化疗及现有靶向治疗的重要原因。
癌症干细胞靶向药物有望增强化疗及放疗对肿瘤细胞的杀伤力5。
参考文献
-
Boman BM, Huang E. Human colon cancer stem cells: a new paradigm in gastrointestinal oncology. J Clin Oncol. 2008;26(17):2828-2838.
-
Jordan CT, Guzman ML, Noble M. Cancer stem cells. N Engl J Med. 2006; 355 (12) : 1253-1261.
-
Hu X, Ghisolfi L, Keates AC,J Zhang, Xiang S, Lee D and Li CJ. Induction of cancer cell stemness by chemotherapy. Cell Cycle, 2012; 11(14):2691-2698
-
Ghisolfi L, Keates AC, Hu X, Lee D and Li CJ. Ionizing radiation induces stemness in cancer cells. Plos One, 2012; 7(8):387-389
-
Li Y, Rogoff HA, Keates S, Gao Y, Murikipudi S, Mikule K, Leggett D, Li W, Pardee AB, Li CJ. Suppression of cancer relapse and metastasis by inhibiting cancer stemness. Proc Nat Acad Sci USA. 2015;112(6):1839-1844.
1.3 癌症干细胞在癌症复发和转移的作用
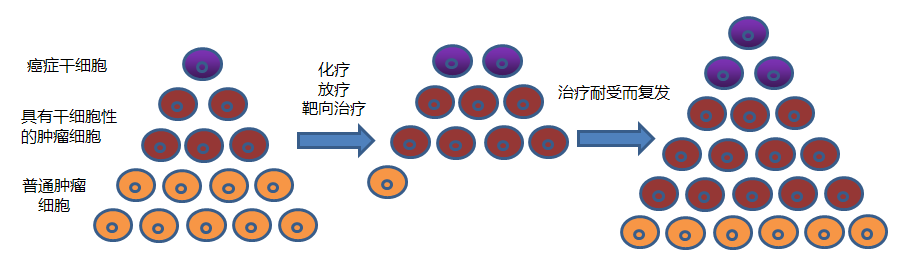
癌症干细胞对化疗具有抗药性1。同时,肿瘤微环境和干性信号通路的失调是癌症干细胞能耐受化疗和放疗的重要原因2。
尽管化疗和放疗可以杀死绝大多数的普通肿瘤细胞,但癌症干细胞并未被根除,从而导致癌症复发及向远处转移3。
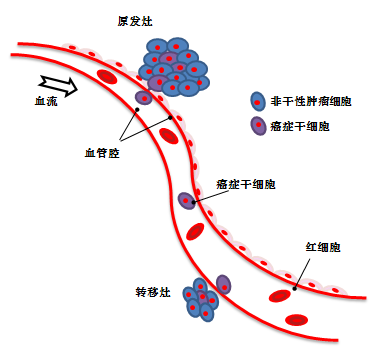
● 癌症干细胞与癌症转移
癌症干细胞具有潜向远处迁移的能力。通过与微环境交互作用,癌症干细胞在远处迁移点仍保持其干细胞性,从而导致转移性肿瘤的生长1,4。
癌症干细胞靶向治疗为癌症治疗带来希望,目前正在开展癌症干细胞通路靶向药物在癌症患者中的安全性和有效性的研究。
癌症干细胞是癌症转移的根源
参考文献
1. Boman BM, Huang E. Human colon cancer stem cells: a new paradigm in gastrointestinal oncology. J Clin Oncol. 2008;26(17):2828-2838.
2. Borovski T, De Sousa E, Melo F, Vermeulen L, Medema JP. Cancer stem cell niche: the place to be. Cancer Res. 2011;71(3):634-639.
3. Jordan CT, Guzman ML, Noble M. Cancer stem cells. N Engl J Med. 2006;355(12):1253-1261.
1.4 文献资料
下列文献有助于进一步深入理解癌症干细胞,我们提供了这些文章的Pubmed链接。
Jordan CT, Guzman ML, Noble M. Cancer stem cells. N Engl J Med. 2006;355(12):1253-1261.